Bristol-Myers Squibb Company obtuvo 18 aprobaciones de nuevos medicamentos y de indicaciones y formulaciones adicionales de medicamentos en 2022.
Esos medicamentos se comercializan actualmente en los principales mercados de la empresa, Estados Unidos y Japón.
Con 34,300 empleados en 44 países, Bristol-Myers Squibb es una empresa biofarmacéutica global cuya misión es descubrir, desarrollar y suministrar medicamentos innovadores que ayuden a los pacientes a vencer enfermedades graves.
Entre sus avances en oncología, la Administración de Alimentos y Medicamentos de los Estados Unidos (FDA) y la Comisión Europea (CE) aprobaron Opdualag, la primera combinación de inhibidor de PD-1 y anticuerpo bloqueador de LAG-3.
Además, en Estados Unidos, la FDA y la CE aprobaron el primer inhibidor de PD-1 y anticuerpo bloqueador de LAG-3.
Estados Unidos, la UE y Japón aprobaron dos regímenes basados en Opdivo como tratamientos de primera línea para el CEC avanzado o metastásico irresecable.
La empresa sigue avanzando e invirtiendo en su cartera de terapia celular mediante la aprobación de Abecma en Japón para el tratamiento del mieloma múltiple en pacientes con al menos tres terapias previas, y las aprobaciones de Breyanzi para el linfoma difuso de células B grandes en recaída o refractario, con tratamientos de segunda línea en Estados Unidos y Japón, y de tercera línea en la UE.
También Bristol-Myers Squibb sigue ampliando sus capacidades de fabricación de terapias celulares en sus instalaciones existentes de Washington y Nueva Jersey, así como mediante la construcción de nuevas instalaciones de fabricación de vanguardia en Massachusetts y en Leiden (Países Bajos).
Nuevos medicamentos
Las autorizaciones de Sotyktu (deucravacitinib) en Estados Unidos y Japón para el tratamiento de la psoriasis en placas de moderada a grave ampliaron su cartera en inmunología.
En el ámbito cardiovascular, la empresa amplió su cartera de nuevos productos con la aprobación por la FDA de Camzyos (mavacamten) para pacientes con MCH obstructiva sintomática.
Además, en agosto de 2022, adquirió Turning Point, una empresa de oncología de precisión, con el objetivo de ampliar su cartera de tumores sólidos con la incorporación de repotrectinib.
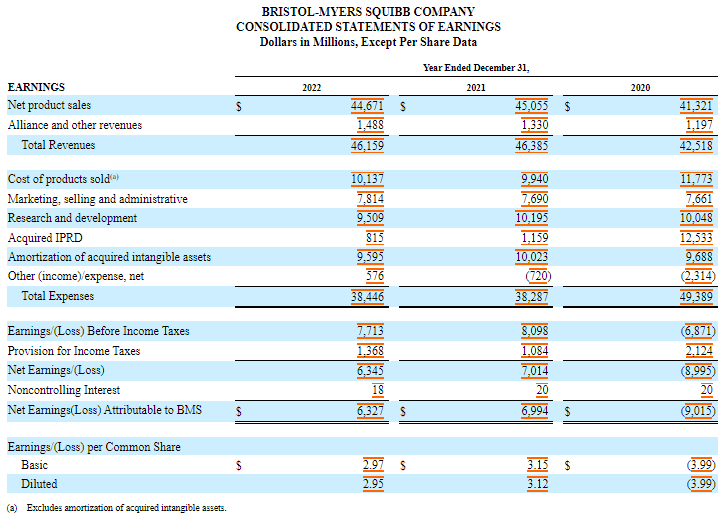
Sus gastos de I+D ascendieron a 9,500 millones de dólares en 2022, 10,200 millones en 2021 y 10,000 millones en 2020.
Los gastos de investigación y desarrollo en curso (IPRD, por su sigla en inglés) adquiridos fueron de 815 millones de dólares, 1,200 millones de dólares y 12,500 millones de dólares en 2022, 2021 y 2020, respectivamente.
En 2020, los IPRD adquiridos incluyeron un cargo de 11,400 millones de dólares resultante de la adquisición de MyoKardia.
![]()

